L’indiana Sun Pharmaceutical ha firmato un accordo definitivo per l’acquisizione di Organon in un’operazione da 11,75 miliardi di dollari cash, pari a 14 dollari per azione della spin off di MSD. L’intesa porterà alla nascita di una nuova realtà industriale, con ricavi combinati stimati in 12,4 miliardi di dollari all’anno, Organon è attiva in oltre 140 Paesi con un portafoglio…
LeggiTag: Sun Pharma
Sun Pharma, cambio al vertice: Kirti Ganorkar nuovo Managing Director
Cambio al verticie di Sun Pharmaceutical Industries, la più grande azienda farmaceutica indiana. Da lunedì 1°settembre Kirti Ganorkar assume la carica di Managing Director, succedendo al fondatore Dilip Shanghvi, che continuerà a essere presente nel Consiglio di Amministrazione dell’azienda nel ruolo di Executive Chairman, con responsabilità sul portafoglio specialistico e sulla strategia di lungo periodo. La nomina di Kirti Ganorkar…
LeggiSun Pharma acquisisce Checkpoint Therapeutics
La pharma indiana Sun Pharmaceutical acquisisce Checkpoint Therapeutics, biotech USA specializzata in immunoterapia e trattamenti oncologici mirati. La parti hanno raggiunto l’accordo sulla base di una cifra iniziale di 355 milioni di dollari, pari al 100% delle azioni di Checkpoint Therapeutics. Con questa operazione entra nel portafoglio di Sun Pharma l’immunoterapia cosibelimab-ipdl (Unloxcyt), approvata dalla FDA per il carcinoma squamocellulare cutaneo…
LeggiSun Pharma: ok FDA a Leqselvi per il trattamento dell’alopecia areata grave
La FDA ha dato l’ok per l’impiego di Leqselvi (deuruxolitinib) di Sun Pharma nel trattamento degli adulti con alopecia areata grave. Leqselvi è uno JAK inibitore: sarà commercializzato in compresse da 8 mg. Il via libera dell’ente regolatorio USA è arrivato sulla base di due studi di fase avanzata, THRIVE-AA1 e THRIVE-AA2, che hanno arruolato un totale di 1.220 pazienti che…
LeggiSun Pharma e Philogen, EMA accetta MMA per Nidlegy (melanoma)
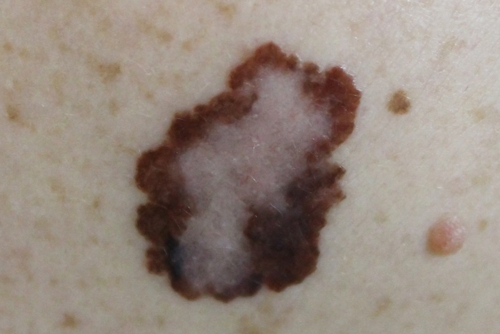
L’EMA ha convalidato la richiesta di autorizzazione all’immissione in commercio (MAA) di Philogen e Sun Pharmaceutical per Nidlegy nel trattamento del melanoma. Nidlegy è una terapia sperimentale neoadiuvante per la cura del melanoma localmente avanzato completamente resecabile. Il prodotto biofarmaceutico è progettato per trattare il cancro della pelle attraverso la somministrazione intralesionale di due principi attivi, L19IL2 e L19TNF, citochine…
LeggiSun Pharma acquisisceTaro Pharmaceutical
Sun Pharmaceutical ha firmato un accordo per l’acquisizione di tutte le azioni ordinarie in circolazione di Taro Pharmaceutical, non attualmente possedute dalla società o dalle sue affiliate. La cifra stabilita è di 347,73 milioni di dollari cash. Taro Pharmaceutical è una biotech israeliana focalizzata sullo sviluppo di farmaci a uso dermatologico non coperti da brevetto. I suoi mercati di riferimento…
LeggiSun Pharma acquisisce Concert Pharmaceuticals
L’indiana Sun Pharma ha completato l’acquisizione di Concert Pharmaceuticals, una società biofarmaceutica statunitense che ha nella propria pipeline deuruxolitinib, potenziale trattamento per pazienti adulti con alopecia areata da moderata a grave. L’operazione si è chiusa a 576 milioni di dollari. “Siamo entusiasti di aggiungere deuruxolitinib, un potenziale trattamento best-in-class per l’alopecia areata in fase avanzata, al nostro crescente portafoglio dermatologico…
LeggiSun Pharma si espande in Giappone con la dermatologia
Sun Pharma ha cominciato la sua attività in Giappone un paio di anni fa acquistando da Novartis una dozzina di farmaci per circa 300 milioni di dollari. Ora sta entrando in possesso di due impianti di produzione e un portafoglio di prodotti dermatologici per 1 milione di dollari in Giappone. Il produttore indiano di farmaci ha infatti annunciato oggi di…
LeggiSun Pharma torna a produrre per gli USA
(Reuters Health) – La più grande casa farmaceutica indiana, Sun Pharmaceutical Industries, ha annunciato la riapertura alla piena produzione – a seguito dell’autorizzazione concessa dalla Food and Drug Administration – del suo impianto di Halol, nell’India occidentale,che era stato sottoposto a restrizioni di fornitura a causa di problemi nel controllo di qualità. Sun sarà ora in grado di riavviare le…
LeggiSun Pharma: FDA dice si a Yonsa. Ha lo stesso principio attivo di Zytiga (J&J)
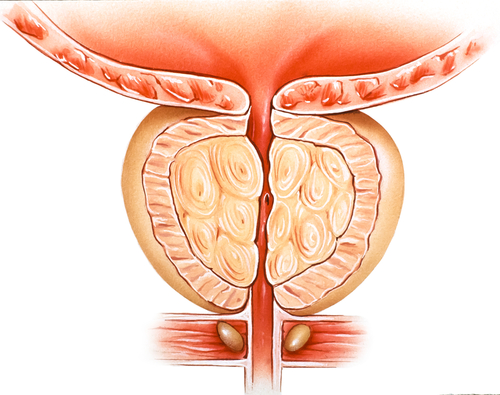
L’indiana Sun Pharma ha ottenuto infatti via libera della FDA per Yonsa, un farmaco contenente lo stesso principio attivo di Zytiga. La sua formulazione, però, non utilizza i brevetti di J & J. Il farmaco è stato approvato in combinazione con metilprednisolone per il trattamento di pazienti con carcinoma prostatico metastatico resistente alla castrazione. Sun Pharma lancerà Yonsa negli Stati…
LeggiSun Pharma, ok da FDA a Ilumya (psoriasi)
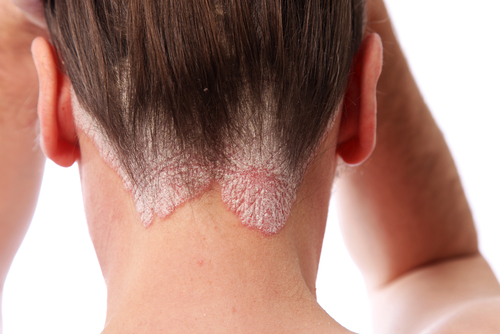
L’accordo da 80 milioni di dollari tra Sun Pharma e MSD nel settore della cura della psoriasi ha dato i suoi frutti: l’ok della FDA per Ilumya, un inibitore di IL-23 prodotto dalla pharma indiana, per curare la psoriasi. Il nuovo farmaco andrà come rivale diretto Tremfya. di J&J. Ilumya può contare su una modalità di somministrazione meno frequente, solo…
LeggiAlmirall-Sun Pharma: tildrakizumab (Sclerosi a placche) sul tavolo dell’EMA
Almirall e Sun Pharma hanno annunciato la deposito del dossier registrativo di tildrakizumab all’EMA da parte di Almirall. Tildrakizumab è un inibitore della IL-23p19 in sperimentazione per il trattamento della psoriasi a placche di grado da moderato a grave. La documentazione comprende i dati di efficacia e sicurezza ottenuti dagli studi “pivotal” di fase III (reSURFACE 1 e 2) che…
Leggi