Lonza ha annunciato un significativo ampliamento delle sue operazioni di produzione in uno dei più grandi impianti di bioconiugazione a livello mondiale, a Visp, in Svizzera. Questo ampliamento è frutto dell’estensione della collaborazione a lungo termine con un partner biofarmaceutico di importanza strategica globale, il cui nome non è stato ancora reso noto. Il nuovo accordo ha l’obiettivo di quadruplicare…
LeggiCategoria: Primo Piano
Cattani: “L’innovazione tecnologica guiderà lo sviluppo di nuove competenze e nuovi bisogni”
Nuove competenze per nuove tecnologie e collaborazione tra tutte le figure Servizio Sanitario Nazionale per affrontare le sfide del futuro. In estrema sintesi è questo il pensiero di Marcello Cattani, Presidente Farmindustria, intervenuto oggi alla cerimonia di apertura del XLIV Congresso Nazionale SIFO che si svolge a Roma dal 5 all’8 ottobre. “La deriva dell’innovazione, sia essa scientifica e tecnologica,…
LeggiDopo lo spin-off da Novartis, Sandoz vale 11 miliardi di dollari
Dopo aver completato ufficialmente la separazione da Novartis, Sandoz ha visto negoziare le sue azioni al SIX Swiss Exchange al prezzo di 24 franchi svizzeri l’una. La valutazione della nuova azienda indipendente è stata fissata a 10,3 miliardi di franchi svizzeri, che equivalgono a circa 11,2 miliardi di dollari, una cifra leggermente inferiore rispetto alle previsioni degli analisti. Sandoz è…
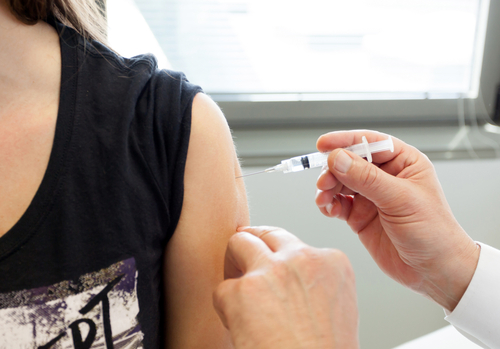
LeggiGiornata Mondiale della meningite, sondaggio internazionale Ipsos: ancora scarsa la consapevolezza. Italia in controtendenza: 9 genitori su 10 si affidano al pediatra per le scelte di vaccinazione
Esiste una scarsa consapevolezza sulla meningite da meningococco e sui sintomi che caratterizzano le fasi iniziali della patologia, spesso rapidissima ad evolvere in poche ore. Questo è il macro-dato che emerge da un sondaggio condotto da Ipsos su oltre 4.000 genitori in USA, Brasile, Germania, Francia, Spagna, Regno Unito e Italia. Il nostro Paese appare all’avanguardia, con nove genitori su…
LeggiRoche: con risdiplam 80% neonati con SMA in piedi dopo un anno di trattamento
Roche ha presentato mercoledì 4 ottobre i risultati positivi dell’analisi primaria dello studio RAINBOWFISH attualmente in corso, volto a valutare l’efficacia e la sicurezza di risdiplam in bambini con atrofia muscolare spinale (SMA) pre-sintomatica (n = 26) tra zero e sei settimane di vita. I dati sono stati presentati al 28° congresso della World Muscle Society (WMS), in corso a…
LeggiProgetto MORe, focus sullo stato dell’arte della salute mentale in Italia
I disturbi mentali ad oggi rappresentano una delle principali fonti di sofferenza e disabilità nel mondo e sono in progressivo aumento. Secondo l’Organizzazione Mondiale della Sanità (OMS), quasi 1 miliardo di persone nel mondo vive con almeno un disturbo mentale (una persona su dieci a livello globale). Si stima, inoltre, che la pandemia COVID-19 abbia incrementato di oltre il 25%…
LeggiBig Pharma, fino al 2030 crescita annuale al 4%
Fino al 2030 il settore farmaceutico assisterà a una crescita stabile sia delle vendite, sia degli utili, nonostante le scadenze dei brevetti che rappresenteranno una sfida. Ne sono convinti gli analisti della banca d’investimento multinazionale americana TD Cowen, che hanno preso in considerazione più di dieci aziende leader per redigere il report Pharma Pulse Q3. Le proiezioni sono più che…
LeggiIl Nobel per la Chimica 2023 agli scopritori dei quantum dot
Il Premio Nobel per la Chimica 2023 va a tre scienziati, Moungi Bawendi, Louis E Brus e Alexey Ekimov per la scoperta dei quantum dot. Si tratta dei più piccoli componenti finora noti nel mondo delle nanotecnologie e le loro possibili applicazioni vanno dai televisori alle lampade a Led fino ai sensori utilizzati nella biomedicina.
LeggiMalaria: Oms raccomanda vaccino per l’immunizzazione dei bambini. È il secondo disponibile nel mondo
L’Organizzazione Mondiale della Sanità (OMS) ha raccomandato un nuovo vaccino, R21/Matrix-M, per la prevenzione della malaria nei bambini. La raccomandazione segue il parere del Gruppo consultivo strategico di esperti sull’immunizzazione (SAGE) e Gruppo consultivo sulle politiche sulla malaria (MPAG) dell’OMS ed è stata approvata dal Direttore generale in seguito alla riunione semestrale tenutasi dal 25 al 29 settembre. L’OMS ha…
LeggiPubblicità, spopolano i famaci per la “diabesità”
Secondo uno studio di MediaRadar – agenzia statunitense di advertising intelligence -nel 2023 sono stati spesi più di 491 milioni di dollari per pubblicizzare farmaci contro la “diabesità”. Un balzo in avanti del 21% rispetto al 2022, anno in cui gli inserzionisti hanno investito 405 milioni di dollari per commercializzare questi prodotti. Ad attrarre gli investimenti più consistenti sono la…
LeggiLa FDA approva antidepressivo first-in-class
La Food and Drug Administration ha approvato Exxua (gepirone cloridrato compresse a rilascio prolungato) per gli adulti con disturbo depressivo maggiore. Exxua, agonista selettivo orale del recettore 1A della serotonina (5HT), è il primo antidepressivo approvato con un nuovo meccanismo d’azione che colpisce selettivamente il recettore 1A della serotonina, un regolatore chiave dell’umore e delle emozioni. Il farmaco è stato…
LeggiBiogen chiude la Digital Health ed esce dall’alleanza con Apple
Biogen ha deciso di chiudere la sua Unit di Digital Health, costituita appena due anni fa. La decisione rientra nell’ambito di un’importante operazione di riduzione dei costi. Per proseguire nel business digital la pharma USA si affiderà a partnership esterne. Si scioglie così l’accordo con Apple, stretto con l’obiettivo di sviluppare biomarcatori digitali della salute cognitiva, basati sui sensori dell’Apple…
LeggiPremio Nobel Medicina 2023 a Katalin Karikó e Drew Weissman per scoperte vaccini a mRna
Il Premio Nobel per la Medicina 2023 va a Katalin Karikó e Drew Weissman per aver scoperto le modifiche delle basi nucleotidiche che hanno consentito lo sviluppo di vaccini mRNA contro il COVID-19. “Attraverso le loro scoperte rivoluzionarie, che hanno cambiato radicalmente la nostra comprensione di come l’mRna interagisce con il nostro sistema immunitario, i vincitori hanno contribuito al ritmo…
LeggiJazz Pharmaceuticals: via libera CE a Enrylaze come componente di un regime chemioterapico multi-agente per il trattamento della LLA e del LBL in pazienti adulti e pediatrici
La Commissione Europea ha rilasciato l’autorizzazione all’immissione in commercio di Enrylaze (JZP458; un’asparaginasi o crisantaspasi ricombinante da Erwinia) come componente di un regime chemioterapico multi-agente per il trattamento della Leucemia Linfoblastica Acuta (LLA) e del Linfoma Linfoblastico (LBL) in pazienti adulti e pediatrici – a partire da 1 mese – che hanno sviluppato un’ipersensibilità o un’ inattivazione silente all’asparaginasi derivata…
LeggiTakeda: ok FDA a somministrazione sottocutanea di Entyvio nella colite ulcerosa
La Food and Drug Administration ha recentemente dato il via libera alla penna preriempita monodose di Entyvio (vedolizumab), prodotta da Takeda, come trattamento per la colite ulcerosa. Questa approvazione consente l’uso del farmaco per via sottocutanea negli adulti che soffrono di colite ulcerosa attiva da moderata a grave, dopo un trattamento iniziale con Entyvio erogato per via endovenosa. Vedolizumab è…
LeggiEgualia: “Con la manovra si dia respiro alle aziende dei farmaci equivalenti”
“Le industrie che producono medicinali equivalenti soddisfano circa il 35% del fabbisogno farmaceutico italiano. Ma necessitano di misure che consentano di continuare a produrre cure che stanno diventando, per le imprese, economicamente non sostenibili. Alcune di queste misure potrebbero trovare spazio nella legge di bilancio, altre hanno bisogno di una programmazione del tempo. È urgente però occuparsene oggi, altrimenti il…
Leggi