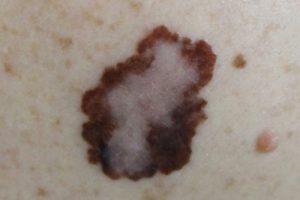
La Commissione Europea ha approvato la commercializzazione di encorafenib e binimetinib in combinazione per il trattamento di pazienti adulti con melanoma inoperabile o metastatico con mutazione BRAF, determinata con test validato.“Siamo molto lieti di annunciare che i pazienti europei con melanoma avanzato con mutazione BRAF avranno a disposizione la combinazione di encorafenib e binimetinib come nuova opzione di trattamento”, dice Frédéric Duchesne, Presidente e CEO della Divisione Farmaceutica di Pierre Fabre. “Tutti noi di Pierre Fabre siamo spinti dal voler fare la differenza in questi pazienti. Con più di 30 anni di esperienza in oncologia e la nostra eredità in dermatologia con la partnership, insieme ad Array BioPharma, siamo stati in grado di indirizzare le nostre conoscenze per aiutare uomini e donne che vivono con questa devastante malattia. La notizia di oggi ci spinge a continuare nella nostra ricerca di innovazione per offrire benefici ai pazienti”.
La decisione della Commissione Europea si basa sui risultati dello studio COLUMBUS di fase III. Questo studio ha dimostrato che la combinazione di encorafenib (450 mg, una volta al giorno) e binimetinib (45 mg, due volte al giorno) ha significativamente migliorato la mediana di sopravvivenza libera da progressione (PFS) rispetto a vemurafenib in monoterapia (960 mg, due volte al giorno). I dati, pubblicati su The Lancet Oncology a settembre, dimostrano che il trattamento con encorafenib e binimetinib ha raggiunto una sopravvivenza globale mediana di 33,6 mesi, rispetto ai 16,9 mesi nei pazienti trattati con vemurafenib in monoterapia (HR 0,61; IC 95%: 0,47–0,79; p<0,0001) nell’analisi pianificata di OS prevista nello studio COLUMBUS. Gli eventi avversi più comuni (≥ 25%), che si sono manifestati nei pazienti trattati con la combinazione di encorafenib e binimetinib alla dose raccomandata (n = 274, sulla base di due studi di fase II e COLUMBUS) erano fatigue, nausea, diarrea, vomito, distacco della retina, dolore addominale, artralgia, aumento di creatinchinasi nel sangue e mialgia. Nello studio COLUMBUS gli eventi avversi che hanno portato a sospensione della terapia per sospetta correlazione al trattamento in studio si sono verificati nel 6% dei pazienti.